Nat Cancer | 清华大学郑撼球课题组揭示MALT1促进肿瘤免疫逃逸的双重机制
AutophagyAdvances
2025-03-15 10:02
文章摘要
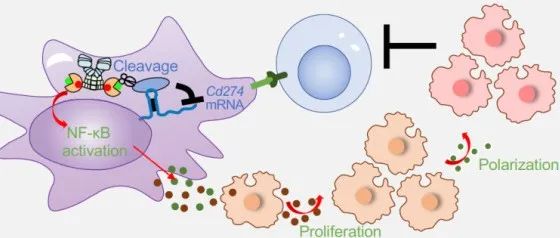
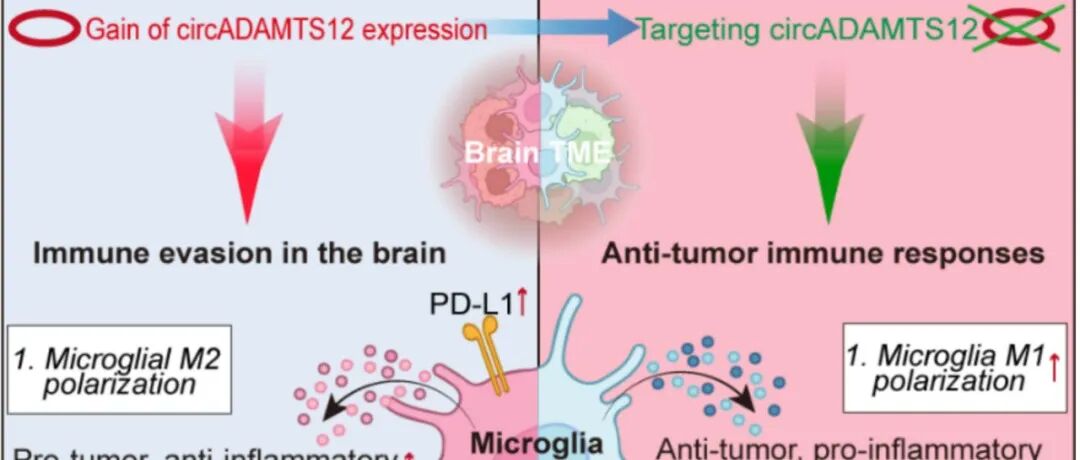
本文介绍了清华大学郑撼球课题组在Nature Cancer上发表的研究,揭示了MALT1通过双重机制促进肿瘤免疫逃逸。一方面,MALT1通过其蛋白酶活性上调PD-L1的表达,使肿瘤细胞抵抗CD8 T细胞的杀伤;另一方面,通过其死亡结构域促进肿瘤相关巨噬细胞的M2型极化,增强肿瘤微环境的免疫抑制性。研究团队利用反义寡核苷酸(ASO)技术靶向MALT1,成功抑制了其双重作用,克服了肿瘤对免疫检查点抑制剂(ICI)疗法的抵抗。这一发现为克服ICI疗法的局限性提供了新的策略,展示了靶向MALT1在临床应用中的潜力。
本站注明稿件来源为其他媒体的文/图等稿件均为转载稿,本站转载出于非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性。如转载稿涉及版权等问题,请作者速来电或来函联系。